从原子结构上如何比较稳定性(原子中电子按照什么规律排列)
导语:从原子的诞生到现在物质的稳定性,从电子排布到泡利原理
颤抖吧化学
今天我们聊一聊化学世界中的微观世界的各种规律!
原子的诞生
我们所在的宇宙诞生于一次大爆炸。大爆炸后约2小时,诞生了大量的氢、少量的氦及极少量的锂。其后,经过或长或短的发展过程,氢、氦等发生原子核的融合反应,分期分批地合成了其他元素

能层与能级
1.能层
(1)含义:在含有多个电子的原子里,由于电子的能量各不相同,因此,它们运动的区域也不同。通常能量最低的电子在离核最近的区域运动,而能量高的电子在离核较远的区域运动。根据多电子原子核外电子的能量差异可将核外电子分成不同的能层(即电子层)。如钠原子核外有11个电子,第一能层有2个电子,第二能层有8个电子,第三能层有1个电子。
在推断题中经常出现与层数有关的概念,理解这些概念是正确推断的关键。为了研究方便,人们形象地把原子核外电子运动看成分层运动,在原子结构示意图中,按能量高低将核外电子分为不同的能层,并用符号K、L、M、N、O、P、Q……表示相应的层,统称为电子层。一个原子在基态时,电子所占据的电子层数等于该元素在周期表中所处的周期数。倒数第一层,称为最外层;从外向内,倒数第二层称为次外层;最内层就是第一层(K层);内层是除最外层外剩下电子层的统称。
2.能级
(1)含义:在多电子原子中,同一能层的电子,能量也可能不同,这样同一能层就可分成不同的能级(也可称为电子亚层)。能层与能级类似于楼层与阶梯之间的关系。在每一个能层中,能级符号的顺序是ns、np、nd、nf……(n代表能层)
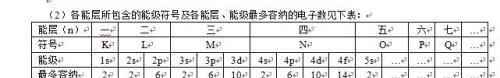
(3)能级数与能层序数的关系
在任一能层,能级数=能层序数。
(4)能级与电子数的关系
以s、p、d、f……排序的各能级可容纳的最多电子数依次为1、3、5、7……的2倍,即2、6、10、14……
说明①在任一个能层中,能级符号顺序为ns、np、nd、nf……(n代表能层),能量依次升高,即在第n层中,不同能级的能量大小顺序是E(ns)<E(np)<E(nd)<E(nf)……
②不同能层,能级符号相同,n越大,能量越高,如E(1s)<E(2s)<E(3s)<E(4s)……

电子云
构造原理
1.构造原理
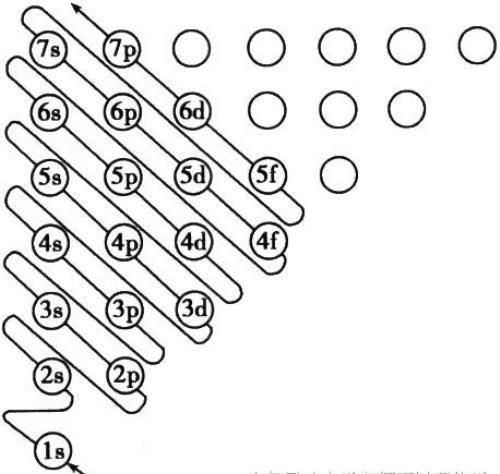
从氢原子开始,随着原子核电荷数的递增,原子核每增加一个质子,原子核外便增加一个电子,电子大多是按图1-1-2所示的能级顺序填充的,填满一个能级再填一个新能级。这个规律称为构造原理。
2.构造原理的应用
构造原理是书写基态原子电子排布式的依据。
将阿拉伯数字放在能级符号前表示能层数,将阿拉伯数字标在能级符号右上角表示该能级上排布的电子数,这就是电子排布式。如N:1s22s22p3,Mg:1s22s22p63s2。
说明 ①电子所排的能级顺序为1s 2s 2p 3s 4s 3d4p 5s 4d 5p 6s 4f 5d 6p 7s……
②图1-1-2中每个小圆圈表示一个能级,每一行对应一个能层。各圆圈间连线的方向表示随核电荷数递增而增加的电子填入能级的顺序。
③构造原理揭示了原子核外电子的能级分布,从中可以看出,不同能层的能级有交错现象,如E(3d)>E(4s)、E(4d)>E(5s)、E(5d)>E(6s)、E(6d)>E(7s)、E(4f)>E(5p)、E(4f)>E(6s)等。
泡利原理和洪特规则

1.泡利原理
在一个原子轨道里,最多只能容纳2个电子,而且它们的自定状态相反(用“↑↓”表示),这个原理称为泡利原理。
电子自旋可以比喻成地球的自转,自旋只有两种方向:顺时针方向和逆时针方向。
2.电子排布图
用方框表示原子轨道,用箭头表示电子(一个箭头表示一个电子),这种用来表达电子排布的新方式叫做电子排布图。
如锂的电子排布图:

3.洪特规则
当电子排布在同一能级的不同轨道时,基态原子中的电子总是优先单独占据一个轨道,而且自旋状态相同。
注意 等价轨道全充满、半充满或全空的状态一般比较稳定,也就是说,具有下列电子层结构的原子是比较稳定的。
全充满:p6、d10、f14,半充满:p3、d5、f7,全空:p0、d0、f0。
因此,铬和铜的基态原子的电子排布图如下:
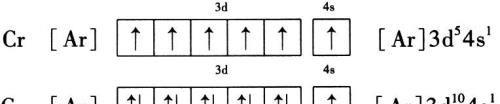
总之,基态原子的电子排布遵循能量最低原理、泡利原理和洪特规则。用构造原理得到的电子排布给出了基态原子核外电子在能层和能级中的排布,而电子排布图还给出了电子在原子轨道中的排布。
这篇文章,估计很多家长都看不太懂,没有事情的啊,可以问问你们高中生的孩子,或者留言给Darren老师!
喜欢Darren老师的点击关注啊!
免责声明:本站部份内容由优秀作者和原创用户编辑投稿,本站仅提供存储服务,不拥有所有权,不承担法律责任。若涉嫌侵权/违法的,请反馈,一经查实立刻删除内容。本文内容由快快网络小面创作整理编辑!