> 美食
溶液的组成方法(溶液组成的表示第二课时教案)
导语:第2节 溶液组成的表示
第2节 溶液组成的表示
一、溶液的组成
1 溶质和溶剂的定义
(1) 溶质:被溶解的物质叫做溶质(溶质可以是固体、液体、气体)
(2) 溶剂:溶解溶质的物质叫做溶剂
例如:
蔗糖溶液:蔗糖是溶质,水是溶剂
碘酒:碘是溶质,酒精是溶剂
酒精溶液:酒精是溶质,水是溶剂
稀盐酸:氯化氢是溶质,水是溶剂
硫酸铜溶液:硫酸铜是溶质,水是溶剂
生理盐水:氯化钠是溶质,水是溶剂
2 溶液的命名:溶质的名称 + 溶剂的名称 + 溶液,除特别说明外,一般人们所说的溶液都是指水溶液,如氯化钠溶液指氯化钠的水溶液
3 溶液的质量 = 溶质质量 + 溶剂质量
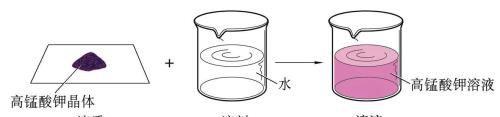
图6-3 溶液的组成
二、溶液浓度的表示
1 溶液的浓度:一定量溶液中所含溶质的量,常用溶液中所含溶质的质量分数来表示
2 溶液的质量 = 溶液的体积×溶液密度
m( 溶液 )=V( 溶液 )×ρ( 溶液 )
三、配制一定溶质质量分数的蔗糖溶液
图6-4 配制蔗糖溶液
1 实验用品:蔗糖,蒸馏水等;托盘天平(含砝码)、纸片、药匙、烧杯、量筒、胶头滴管、玻璃棒等
2 实验过程
本实验欲配制50g溶质质量分数为15%的蔗糖溶液,按以下步骤进行实验:
(1)计算
需要蔗糖的质量为7.5g,需要水的体积为42.5ml
(2)称取蔗糖
(3)量取水
(4)溶解
(5)转移并贴标签(蔗糖溶液,15%)
3 玻璃棒的作用:搅拌,加速溶解
4 使用浓硫酸配制一定溶质质量分数的稀硫酸溶液(稀释前后溶质质量不变),实验步骤:计算,量取浓硫酸和水,配制(稀释),转移并贴标签
本文内容由小娴整理编辑!