氦氖氩原子核外为什么只能排210个电子(氦氖氩氪氙氡核外电子排布)
导语:氦、氖、氩原子核外为什么只能排2、10、18个电子?
氦、氖、氩原子核外为什么只能排2、10、18个电子?
袁玉刚
众所周知,氦、氖、氩原子核外排了2(1s2)、10(1s22s22P6)、18(1s22s22P63s23P6)个电子。但为什么非要这样排呢?就不能有其它排法吗?
按照正统的原子理论和元素周期律,遵循能力最低原理、泡利不相容原理和洪特规则 ,氦、氖、氩原子核外的核外的电子只能这样排布。
He
Ne
Ar
图1 氦、氖、氩原子结构图
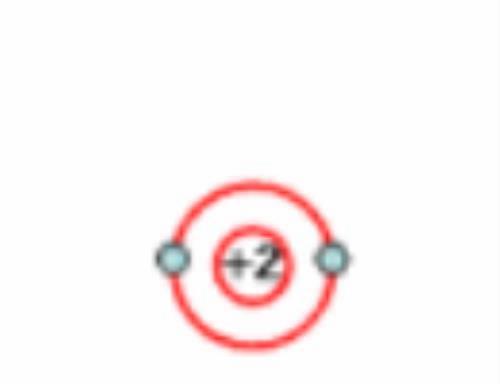
图2 氦原子结构示意图
我试着提出另外一种解释,不知各位朋友能不能接受。
核内核子也可以根据核外电子排布的规律排布,只是增加了中子和相关规则。
1、质子与中子数目相等时原子最稳定,即一夫一妻制时家庭最稳定。
2、核内质子与核外电子相互呼应和纠缠,即孩子跟随母亲。
3、核内核子与核外电子都排布在相应的旋臂和壳层里,即每个粒子都有自己的住处,有道路和院落。
看,这多像摩梭人的母系社会,
氦位于第一层,有两个亚层和两个旋臂,最多只能容纳4个核子。因为有质子与中子数目相等的制约,所以,核内只能排布2个质子,并且对称排布在两个亚层里(11s1、12s1、)。对应的核外电子只能排布2个,但分别位于两个小层里,不需要2个电子自旋方向必须相反的约束。这与正统理论有所区别。所以,氦的电子排布是1×2=2
图3 4He
氖位于第二层,有四个亚层和四个旋臂,最多只能容纳16个核子或者电子。核内只能排布8个质子,并且对称排布在四个亚层里(21s1、、22s1、21P1、22P1、23P1、24P1、25P1、26P1)。其中2P中有4个质子排布在新的旋臂上。所以,氖的电子排布是1×2+2×4=2+8=10。
图4 20Ne
氩位于第三层,有八个亚层和八个旋臂,最多只能容纳64个核子或者电子。核内只能排布32个质子,并且对称排布在八个亚层里。前两个亚层排布着8个质子。
图5 36Ar
质子的排布与核外电子排布一模一样。所以,氩的电子排布是1×2+2×4+4×2=2+8+8=18。
朋友,你看明白了吗?你说,我分析得对不对?
本文内容由小德整理编辑!