> 历史文化
碳酸钠与碳酸氢钠与盐酸反应的现象(碳酸钠和碳酸氢钠与盐酸反应现象)
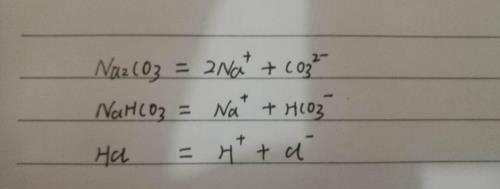
导语:高中化学之碳酸钠和碳酸氢钠与盐酸反应的实质区别解析
碳酸钠(Na2CO3),碳酸氢钠(NaHCO3)与盐酸(HCL)反应的实质区别
很多学生认为,碳酸钠(Na2CO3),碳酸氢钠(NaHCO3)与盐酸反应的产物是一样的,即氯化钠(NaCL),二氧化碳(CO2)和水(H2O),这种理解是完全错误的。
碳酸钠(Na2CO3),碳酸氢钠(NaHCO3)与盐酸(HCL)反应是在溶液中进行的,实质是离子之间的反应,下面我们先看看他们在溶液中的电离情况,如下图:
他们反应的实质其实是溶液中的碳酸氢根离子,碳酸根离子与氢离子之间的反应,而这两个酸根对于的酸是碳酸(H2CO3),碳酸是一种二元弱酸,造成了这两种离子与氢离子的反应有了区别,如下图:
也就是说碳酸根离子与氢离子反应是分步的,第二步才生成碳酸,而碳酸氢根与氢离子反应是直接产生碳酸,那么当氢离子的量较少时,碳酸根离子与氢离子的反应可能只发生了第一步,产物是碳酸氢根离子,就没有碳酸产生。
由此我们也可以得出等浓度的碳酸钠,碳酸氢钠分别与盐酸反应,碳酸氢钠放出二氧化碳的速度快。
总结,如下图:
把这些知识理解了,像“把碳酸钠溶液滴入盐酸溶液中,把盐酸滴入碳酸钠溶液中,把碳酸氢钠溶液滴入盐酸溶液中的现象”这些问题,就迎刃而解了。
学生对这些知识总是容易混淆,掌握不了,专门整理出来,方便学生记忆,使用。希望更多的同学能用上,大家觉得有问题的地方,请及时评论指出,觉得不错的,也请评论,点赞,转发,收藏,留下您的足迹。您的评论是对我最大的支持。
本文内容由小快整理编辑!