> 生活
初中化学-中和反应(中和反应化学式30个)
导语:中考化学复习讲义7——中和反应
酸与碱作用生成盐和水的反应。
一、中和反应定义直接考:
1.中和反应一定有盐和水生成,则有盐和水生成的反应一定是中和反应
2.中和反应属于复分解反应,中和反应是基本反应类型的一种
3.书写化学方程式或离子方程式
二、中和反应的pH坐标曲线图
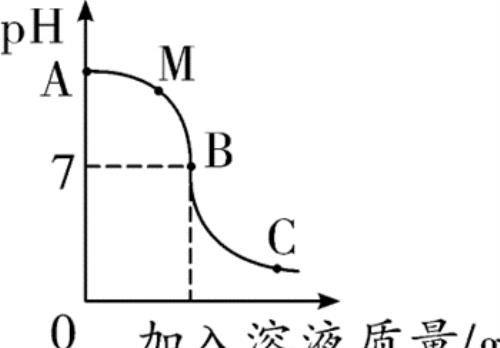
甲图
乙图
①曲线类型判断(看起点和终点)
图解:甲图,A点pH______7,可判断出反应前溶液呈____性(填“酸”或“碱”);B点pH____7,表示_________________;C点的pH____7;可判断出该反应是将______________(填“碱加入酸中”或“酸加入碱中”,下同)。同理可判断出图乙是将___________。
②曲线中各点对应溶液中的溶质判断(以NaOH溶液和稀盐酸反应为例)
甲图
乙图
A点
NaOH
HCl
M点
a._____________
d._____________
B点
b._________
e.________
C点
c.____________
f._____________
三、微观反应示意图
主要是考察书写化学方程式,判断分析反应前后没有变化的离子,反应的实质
四、中和反应的实验相关
1.实验现象和结论
(1)在碱溶液中加入无色酚酞溶液时,出现的现象为__________________。
(2)向含有酚酞的碱溶液中滴加酸,当出现__________________________的现象时,酸碱恰好完全中和。
2.反应后溶液中溶质成分的判断和检验
以Ca(OH)2和HCl的反应为例,若HCl过量,验证方法有:
本文内容由小薇整理编辑!