高中化学有机物的分离与提纯教案(高中化学选修5有机物的分离与提纯)
一、使用干燥剂
1、金属,金属氢化物
Al,Ca,Mg:常用于醇类的干燥.
Na,K:适用于烃,醚,液氨等溶剂的干燥。
醇中有微量的水分可加少量金属钠直接蒸馏。
CaH:比碱金属、五氧化二磷干燥效果好。适用于烃,卤代烃,醇,醚等
LiAlH4:常用醚类等溶剂的干燥。
2、中性干燥剂
CaSO4,Na2SO4,MgSO4:适用于烃及烃的衍生物的干燥。
CuSO4:无水硫酸铜为白色,含有5个分子的结晶水时变成蓝色,常用检测溶剂中微量水分。CuSO4适用于醇,醚,酯,低级脂肪酸的干燥。
【注意】甲醇与CuSO4能形成加成物,故不宜使用。
CaC2:适用于醇干燥。纯度差的碳化钙,会有硫化氢和磷化氢等恶臭气体
CaCl2:适用于干燥烃,卤代烃,醚,硝基化合物,二硫化碳等。
活性氧化铝:适用于烃,酯的干燥。
分子筛:吸湿能力仅次于五氧化二磷。几乎都可以用在实验室和工业上。

3、碱性干燥剂
KOH,NaOH:适用于碱性物质。酸,酚,醛,酮,醇,酯等不适用。
K2CO3:适用于碱性物质及卤代烃,醇,酮,酯等。不适用于酸性物质。
BaO,CaO:用于醇及碱性物质。不用于酮,酸性物质和酯类。
4、酸性干燥剂
H2SO4:适用于干燥饱和烃,卤代烃,硝酸,溴等。醇,酚,酮,不饱和烃等不适用。
P2O5:适用于烃,卤代烃,酯,乙酸,二硫化碳,液态二氧化硫的干燥。醚,酮,醇等不适用。
二、蒸发、蒸馏、分馏
沸点与水的沸点相差较大的溶剂可以用分馏效率高的蒸馏塔(精馏塔)。
1、共沸蒸馏脱水
与水生成共沸物的溶剂不能采用分馏脱水的方法。如果含有极微量水分的溶剂,通过共沸蒸馏,虽然溶剂有少量的损失,但却能脱去大部分水。一般多数溶剂都能与水组成共沸混合物。
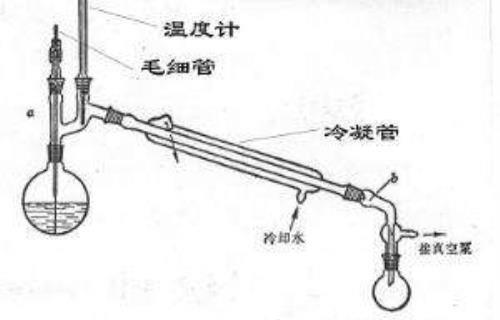
2、减压蒸馏
进行干燥的溶剂很难挥发而不能与水组成共沸混合物的,可以通过加热或减压蒸馏使水分优先除去。例如,醇,甘油等溶剂都适用。
3、用干燥的气体进行干燥
将难挥发的溶剂乙二醇,甘油等溶剂的干燥,可吹入充分干燥的空气或氮气,气体带走溶剂中的水分。
4、在特殊情况下,用乙酸酐干燥或无水硼酸进行脱水干燥。
三、冷却干燥
冷却干燥的方法:如烃类用冷冻剂冷却,其中水分结成冰而脱水。
免责声明:本站部份内容由优秀作者和原创用户编辑投稿,本站仅提供存储服务,不拥有所有权,不承担法律责任。若涉嫌侵权/违法的,请与我联系,一经查实立刻删除内容。本文内容由快快网络小纳创作整理编辑!