原子核的组成和结构(原子的组成和结构图)
导语:原子核的组成
一、天然放射现象
1896年,法国物理学家贝克勒尔发现,轴和含轴的矿物能够发出看不见的射线,它能穿透黑纸使照相底版感光。受到贝克勒尔的发现的鼓舞,波兰裔法国物理学家玛丽·居里和她的丈夫皮埃尔·居里

对轴和含轴的各种矿石进行了深入研究。他们发现了一种沥青中的含铀物质,根据它的含轴量计算发出的射线不会太强,但实际测得的射线要强得多。进一步研究后,发现这种沥青中还存在着两种能够发出更强射线的新元素,居里夫人把其中一种元素命名为钋(Po),另一种元素命名为镭(Ra)。
物质发出射线的性质称为放射性(radioactivity),具有放射性的元素称为放射性元素。后来发现,放射性并不是少数元素才有的,原子序数大于83的元素,都能自发地发出射线,原子序数小于或等于83的元素,有的也能发出射线。放射性元素自发地发出射线的现象,叫作天然放射现象。
二、射线的本质
发现了天然放射现象之后不久,人们就在想,这些射线到底是什么呢?
把放射源轴、钋或镭放入用铅做成的容器中,射线只能从容器的小孔射出,成为细细的一束。若在射线经过的空间施加磁场,可以发现射线分裂成三束,其中两束在磁场中向不同的方向偏转,这说明它们是带电粒子流;另一束在磁场中不偏转,说明它不带电(图)。
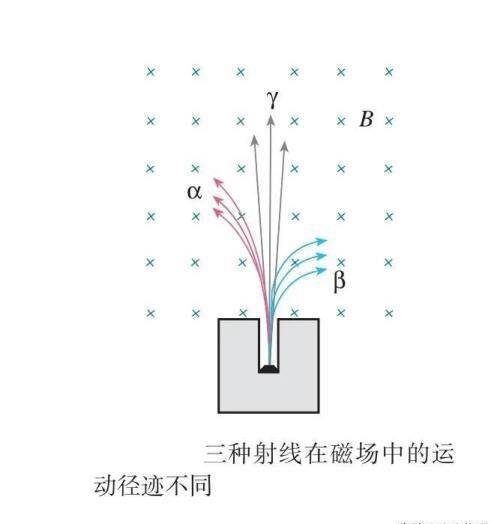
于是,人们把这三种射线分别叫作α射线、射线和y射线。
☞[what]如果α射线、β射线都是带电粒子流,按照图中标出的径迹判断,它们分别带什么电荷?
如果不用磁场而用电场判断它们带电的性质,两个电极怎样放置可以使三种射线大致沿图示的方向偏转?
物理学家们经过多方面的研究后确认α射线、β射线和γ射线具有以下特征。
α射线 是高速粒子流,粒子带正电,电荷量是电子的2倍,质量是氢原子的4倍,其组成与氦原子核相同。α粒子的速度可以达到光速的1/10。由于α粒子带电,质量又比较大,通过气体时很容易把气体分子中的电子剥离,使气体电离。由于与物质中的微粒作用时会损失自己的能量,α粒子穿透能力较弱,在空气中只能前进几厘米,用一张纸就能把它挡住。
β射线 是高速电子流,它的速度更大,可达光速的99%。它的电离作用较弱,穿透能力较强,很容易穿透黑纸,也能穿透几毫米厚的铝板。
γ射线 是能量很高的电磁波,波长很短,在10⁻¹⁰m以下。它的电离作用更弱,穿透能力更强,甚至能穿透几厘米厚的铅板和几十厘米厚的混凝土。实验发现,如果一种元素具有放射性,那么,无论它是以单质存在的,还是以化合物形式存在的,都具有放射性。放射性的强度也不受温度、外界压强的影响。由于元素的化学性质决定于原子核外的电子,这就说明射线与这些电子无关,也就是说,射线来自原子核。这说明原子核内部是有结构的。
α射线、β射线都是高速运动的粒子,能量很高,γ射线是波长很短的光子,能量也很高。
☞从原子内部能够射出这样高能的粒子,这使人们意识到原子核是一个能量的宝库。
☞射线使原子中的电子脱离核的束缚成为自由电子,这样的过程叫作电离。射线的上述作用叫作电离作用。

三、原子核的组成
1919年,卢瑟福用镭放射出的α粒子轰击氮原子核,从氮原子核中打出了一种新的粒子(图)。
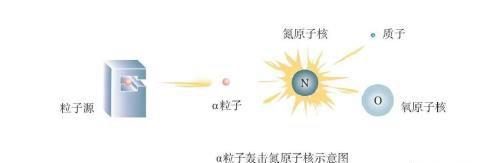
根据这种粒子在电场和磁场中的偏转,测出了它的质量和电荷量,原来它就是氢原子核,叫作质子(proton),用p表示。以后,人们用同样的方法从氟、钠、铝等原子核中都打出了质子,由此断定,质子是原子核的组成部分。
质子带正电荷,电荷量与一个电子的电荷量相等。质子的质量为
mp=1.672621898×10⁻²⁷kg
☞[what]原子核是只由质子组成的吗?如果原子核中只有质子,那么,任何一种原子核的质量与电荷量之比,都应该等于质子的质量与电荷量之比。但事实是这样的吗?
实际情况并非如此。绝大多数原子核的质量与电荷量之比都大于质子的相应比值。卢瑟福猜想,原子核内可能还存在着另一种粒子,它的质量与质子相同,但是不带电,他把这种粒子叫作中子(neutron)。1932年,卢瑟福的学生查德威克通过实验证实了这个猜想(图)。
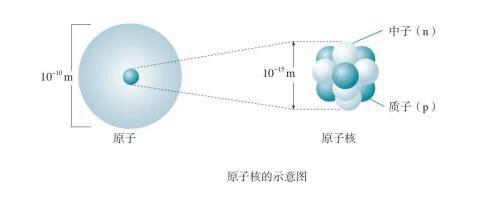
中子不带电,用n表示。中子的质量是
mn=1.674927471×10⁻²⁷kg
它与质子的质量非常接近,只比质子质量约大千分之一。质子和中子除了是否带电的差异以及质量上的微小差别外,其余性质十分相似,而且,都是原子核的组成成分,所以统称为核子(nucleon)。
由于中子不带电,原子核所带的电荷等于核内质子电荷的总和。所以,原子核所带的电荷总是质子电荷的整数倍,通常用这个整数表示原子核的电荷量,叫作原子核的电荷数,用Z表示。原子核的质量等于核内质子和中子的质量的总和,而质子与中子的质量几乎相等,所以原子核的质量几乎等于单个核子质量的整数倍,这个倍数叫作原子核的质量数,用A表示。
原子核的电荷数就是核内的质子数,也就是这种元素的原子序数,而原子核的质量数就是核内的核子数。原子核常用符号ᴬᴢX表示(图),

X为元素符号,A表示核的质量数,Z表示核的电荷数(即原子序数)。
☞原子核的电荷数不是它所带的电荷量,质量数也不是它的质量。
例如,氢原子核可以表示为¹₁H,有时也用它表示质子。
氦原子核可以表示为⁴₂He,它有2个质子和2个中子,所以电荷数是2,质量数是4。又如,²³⁸₉₂U代表一种轴核,它的质量数为238,电荷数为92,即核内有92个质子、146个中子。
元素的性质与原子核外的电子有密切的关系。同种元素的原子,质子数相同,核外电子数也相同,它们就会具有相同的化学性质。但是,它们的中子数可能不同。这些具有相同质子数而中子数不同的原子核组成的元素,在元素周期表中处于同一位置,因而互称同位素(isotope)。
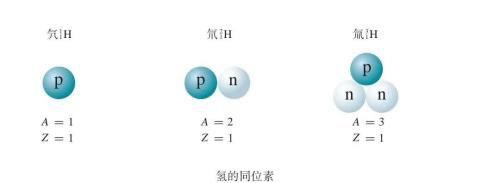
氢有三种同位素,分别叫作氕(也就是通常说的氢)、氘(也叫重氢)、氚(也叫超重氢),符号分别是¹₁H、²₁H、³₁H(图)。


免责声明:本站部份内容由优秀作者和原创用户编辑投稿,本站仅提供存储服务,不拥有所有权,不承担法律责任。若涉嫌侵权/违法的,请与我联系,一经查实立刻删除内容。本文内容由快快网络小媛创作整理编辑!