Angew: Ni3Sn2-NiSnOx纳米复合电催化剂促进HER

全文简介
实现高效的水解吸附、易于脱附的OH-和易于形成氢-氢键的电催化剂,在实现高效碱性制氢反应(HER)方面至关重要,但也具有挑战性。在此,我们提出了 Ni3Sn2-NiSnOx 纳米复合材料的设计以解决这一挑战。我们展示了 Ni3Sn2 具有理想的氢吸附和低水氢离子吸附能力,而NiSnOx则有助于水分解和氢氧离子转移过程。因此,两个功能部分之间精细调节的相互作用实现了多个功能之间的协调,并显著提高了 HER 动力学效率。在优化的催化剂上,仅需要 14 和 165 mV 的过电位,即可得到10和1000 mA / cm² 的电流密度。本研究凸显了考虑活性位点与所有相关中间体之间固有相互作用对获得有前途的电催化剂的重要性。
结果与讨论
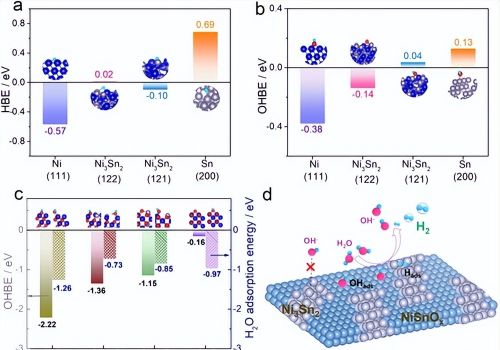
图1 a)计算Ni(111)、Ni3Sn2(122)、Ni3Sn2(121)和Sn(200)表面的h结合能(OHBEs, ΔEH)和b) oh结合能(OHBEs, ΔEOH)。c)计算出金属氧化物在不同表面上的ohbe和H2O吸附能。蓝色、红色、灰色和小天蓝色球体分别代表Ni、O、Sn和H原子。d)协同Ni3Sn2-NiSnOx电催化剂碱性HER过程预测示意图。
我们首先通过密度泛函理论计算研究了金属成分或金属氧化物对H*、OH-和H2O物种的吸附能力。如图1a所示,我们在Ni3Sn2 (122) 和Ni3Sn2 (121) 表面上获得的H结合能(HBE)值分别为0.02和-0.10 eV,比Ni (111) 表面的-0.57 eV和Sn (200) 表面的0.69 eV更接近于H2发生反应的最优值。图1b显示了这些金属表面的OH结合能(OHBE)值的计算结果。Ni (111) 表面的OHBE为-0.38 eV,表明金属Ni具有吸附OH-物种的能力,这可能会干扰H*物种与活性位点的相互作用。通过与弱氧亲和力的Sn中和形成金属间化合物Ni3Sn2,OHBE值明显调节为Ni3Sn2 (122) 和(121)表面的-0.14和0.04 eV,这些结果共同预示着Ni3Sn2作为H2发生反应的功能组分的卓越性,因为它具有有利于易于生成H2的氢-氢键形成的HBE和易于减轻OH-竞争吸附在H2发生反应位点上的正OHBE。然后计算了NiSnOx双金属氧化物表面上OH-和H2O的吸附能量。结果清楚地显示,将Sn掺入NiO中可以调节OH-和H2O在潜在稳定表面上的吸附能量(如图1c所示),使其既不过弱,以致无法进行H-OH解离吸附,也不过强,以至于阻塞活性位点进行后续催化反应,这使得NiSnOx比NiO更有效地促进碱性制氢反应中H2O分解和OH转移过程。这些理论结果表明,将Sn与Ni以金属间化合物Ni3Sn2或NiSnOx双金属氧化物的形式结合起来可以调节它们与碱性制氢反应中涉及的所有相关吸附物种之间的内在相互作用。因此,合理混合这两个组分有望实现高效的水解吸附、易于脱附的OH-和易于形成氢-氢键的碱性制氢反应,如图1d所示。
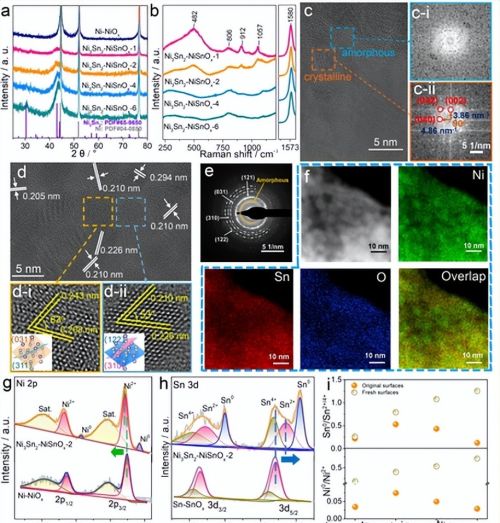
图2 a) Ni3Sn2-NiSnOx-m与Ni-NiOx电极的XRD谱图,b) Ni3Sn2-NiSnOx-m催化剂的拉曼光谱(以碳为内标,G波段为1580 cm−1)。c)和d) Ni3Sn2-NiSnOx-2电催化剂的球差校正HRTEM图像,c-i)和c-ii)是所选代表性非晶NiSnOx和(c)中标记的结晶Ni3Sn2结构域对应的FFT图,(d-i)和(d-ii)是(d)中标记的所选结晶结构域。(d-i)和(d-ii)的插入分别是Ni3Sn2的不同平面间夹角的晶体结构。e) SAED图,f) Ni3Sn2-NiSnOx-2催化剂HAADF-STEM图和元素映射图。Ni3Sn2-NiSnOx-2催化剂以及Ni- niox和Sn- snox样品的g) Ni 2p和h) Sn 3d区域的高分辨率XPS光谱。i)从制备的Ni3Sn2-NiSnOx-m样品(原始表面)获得的表面Ni0/Ni2+和Sn0/Sn2+/4+的比率,以及在XPS测量过程中原位去除暴露在空气中的表面成分后的样品(新鲜表面)。
Ni-NiOx的X射线衍射(XRD)图案仅显示出与典型金属Ni有关的衍射峰(图2a)。至于Ni3Sn2-NiSnOx-m电极,则除了与Ni相关的那些之外,主要观察到相对宽化且低强度的衍射峰,在30.4°、42.9°和44.1°处(图2a)对应于Ni3Sn2。此外,Ni3Sn2的XRD峰相对于Ni强度随着Sn/Ni进料比的增加而增加,表明样品中Ni3Sn2部分的相对量增加;此外,由于在XRD图案中未检测到金属氧化物的信号,因此可以合理地推断Ni3Sn2-NiSnOx-m的NiSnOx组分是非晶的。这些结果共同表明Ni3Sn2-NiSnOx-m样品由晶态Ni3Sn2和非晶态NiSnOx双组分组成,而Ni3Sn2的相对含量随着Sn/Ni进料比的增加而增加,NiSnOx的相对含量则减少。
通过球差校正的HRTEM(AC-HRTEM)分析获得了有关催化剂原子级结构的更多见解。放大的AC-HRTEM图像显示晶态Ni3Sn2 NP和非晶态NiSnOx组分之间明显的界面,通过相应的选择区域快速傅里叶变换(FFT)模式进一步验证,非晶态区域显示模糊的环形,晶态区域则显示亮点(图2c,图S14和S15)。这些结果共同表明Ni3Sn2 NPs中的多晶领域具有不同的晶面,这一点通过选择区域电子衍射(SAED)图案进一步确认(图2e)。SAED图案上出现高度模糊的光晕,被归为非晶态NiSnOx组分。高角暗场扫描透射电子显微镜(HAADF-STEM)图像和EDS映射(图2f)进一步揭示了Ni3Sn2-NiSnOx-2催化剂明确定义的纳米复合体。
性能测试
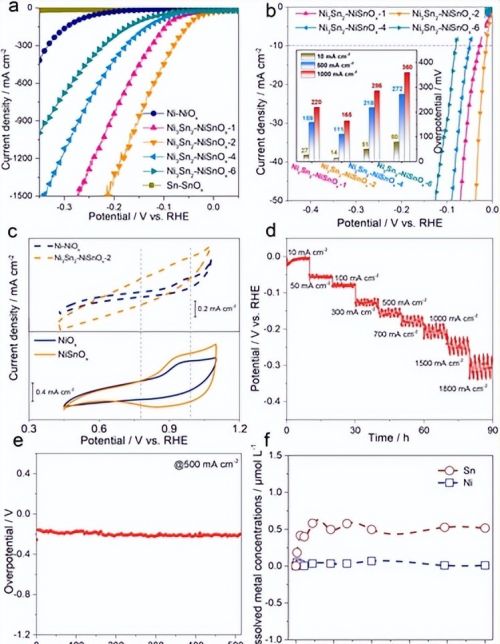
图3 a)和b)不同样品在1 M KOH电解液中25°C时的线性扫描伏安曲线。(b)图为Ni3Sn2-NiSnOx-m样品在不同电流密度下的过电位图。c)扫描速率为1 mV s−1时,不同样品在1 M KOH条件下的CV曲线。d)多电流过程和e) Ni3Sn2-NiSnOx-2催化剂在1 M KOH电解液中25°C下电流密度为500 mA cm−2时的时间电位曲线。实验结果采用90% ir补偿。f)等离子体质谱(ICP-MS)测定的电解液中溶解的Ni和Sn离子浓度。
评估了Ni3Sn2-NiSnOx-m催化剂与Ni-NiOx和Sn-SnOx在碱性HER方面的性能。如图3a所示,Sn-SnOx不是一种高效的碱性HER电催化剂。至于Ni-NiOx,其过电位分别为162和362 mV时,可获得电流密度为10和500 mA cm-2。在引入Sn后,Ni3Sn2-NiSnOx-m催化剂的HER活性显著提高。此外,循环伏安(CV)曲线的两对比较(图3c)表明,Ni3Sn2-NiSnOx-2和NiSnOx在形成(由H-OH解离吸附产生)和解离(从OH转化为OH-)OH物种方面与Ni-NiOx和NiOx相比具有明显的可逆性(OHad区域:0.60 <E <1.00 V)。与金属氧化物相比,Ni-NiOx和Ni3Sn2-NiSnOx-2的电流范围较小,这可以归因于它们增强的OH转移过程,这对于HER动力学是有益的。这些结果证实了Ni3Sn2-NiSnOx复合体对于碱性HER具有优异的性能,这与DFT预测相一致。对于Ni3Sn2-NiSnOx-m催化剂,观察到其活性随着Sn/Ni进料比的增加而最初增加然后降低(图3a和b)。其中,Ni3Sn2-NiSnOx-2表现出了最高的HER性能。在微小的过电位下,分别实现了10、500和1000 mA cm-2的电流密度,其过电位分别为14、111和165 mV。
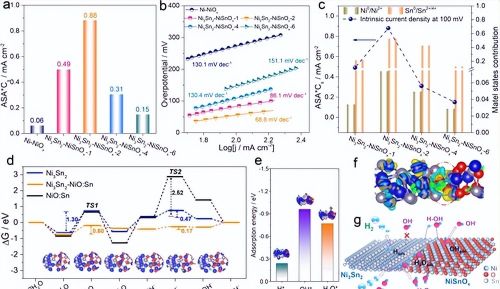
图4 a)在100 mV下用ecsa正态化电流密度得到的催化剂的内在比活性。b)不同电催化剂的Tafel图。c) Ni3Sn2-NiSnOx-m电极的本征活性与异质界面性质(由XPS分析计算的Ni0/Ni2+和Sn0/Sn2+/4+比值)的关系。d) Ni3Sn2、NiO: Sn (Sn掺杂NiO)和Ni3Sn2-NiO: Sn模型上碱性HER的能量谱。过渡状态。图中为Ni3Sn2-NiO: Sn模型在碱性HER反应过程中中间体的俯视图结构。e)不同物质在Ni3Sn2-NiSnOx上的吸附能。f) Ni3Sn2-NiSnOx复合材料的电荷密度差。黄色和绿色区域分别代表电子消耗和积累。g) Ni3Sn2-NiSnOx纳米复合材料的HER机理示意图。
通过电化学表面积(ECSA)对催化剂的内在特异活性进行归一化处理,发现Ni3Sn2-NiSnOx-m催化剂的内在活性(ASA*Cs)随着Sn/Ni投料比例的增加而先增后降。通过之前的分析,可以发现随着Sn/Ni投料比例的增加,Ni3Sn2组分的相对含量增加,NiSnOx的相对含量减少。这表明Ni3Sn2-NiSnOx-m的内在活性显然受到Ni3Sn2和NiSnOx双组分相对含量的影响。此外,研究者还发现Ni3Sn2-NiSnOx-m电极的内在HER活性与金属Ni0和Sn0的贡献呈正相关,这与所制备电极表面的异面界面性质有关,表明碱性HER是一种依赖于Ni3Sn2-NiSnOx-m催化剂的异面界面反应,充足的异面界面对反应有益。
为了进一步研究碱性HER机理以及Ni3Sn2-NiSnOx复合材料中双重功能组分如何影响反应动力学,因此绘制了Ni3Sn2、NiSnOx和Ni3Sn2-NiSnOx碱性HER的Gibbs自由能图谱(图 4d)。 碱性HER经历两个关键步骤,第一个是初始H2O解离以生成伴随OH转移过程的H中间体,第二个是H物种电化学偶联脱附以产生H2发展。 对于Ni3Sn2,DFT计算的H2O解离能垒为1.30 eV,确认其对于H2O解离过程具有低催化活性。 因此,尽管已证明Ni3Sn2对于H2发展过程(图 1a和b)具有益处,具有低的H2形成能垒0.47 eV,但在碱性环境下它表现出差的HER活性。这些结果在理论上揭示了单个Ni3Sn2或NiSnOx即使它们各自具有出色的电子性质(图 1)也难以有效催化碱性HER,与实验结果相一致。 在形成Ni3Sn2-NiSnOx复合材料后,界面处的电荷密度差显然被重新分布(图 4f),表明从NiSnOx到Ni3Sn2的电子转移。 这种调制增加了Ni3Sn2的电负性和NiSnOx的电正性,进一步调节了相关吸附物的结合能(H,OH和H2O分别为−0.24、−0.96和−0.77 eV,图 4e)。 然后,DFT计算揭示了在Ni3Sn2 / NiO:Sn界面处显着降低能量障碍的明显提高的H2O解离和OH传递过程,表明了Ni3Sn2-NiSnOx纳米复合材料对于加速催化动力学的优越性。 这些结果共同揭示了Ni3Sn2-NiSnOx复合材料的碱性HER机理:初始的H2O分子在Ni3Sn2 / NiSnOx异质界面上进行解离吸附,而产生的H物种首选在Ni3Sn2/NiSnOx界面的Ni位置上吸附。同时,NiSnOx组分中由相邻Sn修饰的Ni位点用作OH吸收剂以承载生成的OH物种。 之后,H物种从Ni3Sn2组分的活性Ni位点快速电化学脱附以产生H2。同时,选择地吸附在NiSnOx组分修饰的Ni位点上的OH*物种有效地转移用于后续反应(图4g)。 这清楚地解释了为什么Ni3Sn2-NiSnOx-m的实验观察到的HER性能强烈取决于Ni3Sn2和NiSnOx组分的相对含量。平衡这两个功能组分,可以实现Ni3Sn2-NiSnOx-2的互相协调,以有效解离吸附水,轻松脱附OH-并同时促进氢键结合,从而提高了碱性HER性能。
结论
总的来说,设计并构建了Ni3Sn2-NiSnOx纳米复合材料催化剂,实现了高效的碱性HER。实验和理论结果表明,Ni3Sn2是H2形成的理想活性组分,而NiSnOx组分能够有效加速水解离和OH传递过程。因此,在两个组分之间进行合理耦合,实现了在水的高效解离吸附,OH-的易于脱附和氢键结合的同时促进,从而显著提高了复合材料催化剂的反应动力学。因此,最佳的Ni3Sn2-NiSnOx复合材料在碱性HER中表现出非常小的超电势,为10和1000 mA cm-2的电流密度分别提供14和165 mV,与最先进的无贵金属催化剂的阳极相当。这项工作不仅提供了一种合理的方法,用于设计优秀的碱性HER电催化剂,而且开发出了大规模H2生产的可行替代方案。
参考文献
Yang, J., Shen, Y., Sun, Y., Xian, J., Long, Y., Li, G., Angew. Chem. Int. Ed. 2023, 62, e202302220; Angew. Chem. 2023, 135, e202302220.