第一电子电离能规律(高中化学第一电离能图)
化学干货II高中化学电子排布、第一电离能和电负性知识汇总
一、原子结构
1.原子的组成:原子核、核外电子
2.原子的特点:
原子不显电性,体积小,质量小,质量主要集中在原子核上,原子核的密度非常大
3.核外电子排布规律
(1)能量最低原理
(2)每一层最多容纳电子数:2n2个
(3)最外层电子数不超过8个(K层为最外层时不超过2个)
(4)次外层电子数不超过18个,倒数第三层不超过32个
二、能层与能级
能量最低原理:原子的电子排布遵循能使整个原子的能量处于最低状态
基态原子:处于最低能量的原子
1.能层:核外电子的能量是不同的,按电子能量差异,可以将核外电子分成不同的能层——电子层
同一能层的电子,能量也可能不同,还可以分成不同能级能级数
2.能级:s、p、d、f····
以s、p、d、f····排序的各能级可容纳的最多电子数依次为1、3、5、7、······的二倍。
能级数=能层序数(n)
三、构造原理
1.电子排布式
Na:1s22s22p63s1
试书写N、Cl、K、26Fe原子的核外电子排布式
注意:
24Cr:1s22s22p63s263d54s1
29Cu:1s22s22p63s2263d104s1
离子电子排布式书写——先失去最外层电子与能量最低原则无关
1)、能量最低原理
2)、每个原子轨道上最多能容纳__2__个电子,且自旋方向__相反____(泡利不相容原理)
3)、当电子排布在同一能级时,总是__首先单独占一个轨道__,而且自旋方向_相同__。(洪特规则)
4)、补充规则:全充满(p6,d10,f14)和半充满(p3,d5,f7)更稳定
2.简化电子排布式
15P:[Ne]3s23(表示内层电子与Ne相同。与上层稀有气体的核外电子排布相同)
29Cu:[Ar]3d104s1
3.外围电子(价电子)
价电子层:电子数在化学反应中可发生变化的能级
主族元素的性质由最外层电子决定
过渡元素的性质由最外层电子和次外层电子决定
四、电子云与原子轨道
1、电子云:电子在原子核外出现的概率分布图
2.原子轨道:s、p、d、f电子轨道形状
3.原子的电子排布图
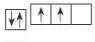
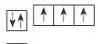
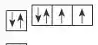
五、能量最低原理、基态与激发态、光谱
基态原子:处于最低能量的原子 (稳定)
激发态原子:基态原子的电子吸收能量后电子会跃迁到较高的能级,变为激发态原子
原子光谱:不同元素的原子发生跃迁时会吸收或释放不同的能量,表现为光的形式得到各种元素的电子的吸收光谱或发射光谱可利用原子光谱上的特征谱线来鉴定元素,称为光谱分析。
六、原子结构与元素周期表
周期数=电子层数
主族序数=外围电子数=最外层电子数
大多数副族序数=外围电子数=(n-1)d+ns的电子数
区的划分
除ds区外,区的名称来自按构造原理最后填入电子的能级的符号
s区元素:结构特点:ns1和ns2
包括ⅠA族和ⅡA族 除氢外均为金属
P区元素:结构特点:ns2np1-6
包括ⅢA族-ⅦA族和0族 绝大多数为非金属
d区元素:结构特点:(n-1)d1-9ns1-2
包括ⅢB族-ⅦB族和第Ⅷ族 全部是金属
ds区元素:结构特点:(n-1)d10ns1-2
包括ⅠB族和ⅡB族 全部是金属
f区元素:包括镧系和锕系
d区、ds区和f区元素称过渡元素
练习1.下列元素是主族元素还是副族元素?第几周期?第几族?
(1)1s22s2 2p6 3s2 5
(2)[Ar]3d104s1
2.由下列元素在周期表中的位置,给出其原子的价电子层构型
(3)第四周期第ⅥB族 (4)第六周期第ⅡA族
七、元素的性质
1、主要化合价:最高正价=最外层电子数=主族序数
负化合价= 最外层电子数–8
2、元素的金属性、非金属性:金属性左下;非金属性右上
3、原子半径:层数、质子数
4、电离能:
气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量叫做第一电离能。
用符号I1表示.
衡量元素的原子失去一个电子的难易程度。
第一电离能数值越小,原子越容易失去一个电子;反之越难
同周期从左往右越来越大(二五族反常),同主族从上往下越来越小
5、电负性:
用来描述不同元素的原子对键合电子吸引力的大小。电负性越大的原子,对键合电子的吸引力越大。
同周期从左往右越来越大,同主族从上往下越来越小
电负性越大,元素的非金属性越强,电负性越小,元素的非金属性越弱,金属性越强
一般:非金属>1.8 金属<1.8 类金属≈1.8
电负性相差很大的元素化合通常形成离子键,电负性相差不大的两种非金属元素化合,通常形成共价键。
成键元素原子的电负性差>1.7,离子键 成键元素原子的电负性差<1.7,共价键
温馨提示:通过以上关于化学干货II高中化学电子排布、第一电离能和电负性知识汇总内容介绍后,相信大家有新的了解,更希望可以对你有所帮助。