初中化学离子符号怎么写(初三化学离子符号记忆口诀)
考点透析
一、离子
1 定义
带电的原子或原子团叫做离子。
2 形成
元素的原子在发生化学反应时都有一个趋势:通过得失电子使自己的最外层达到相对稳定的结构。具体过程如下图所示:
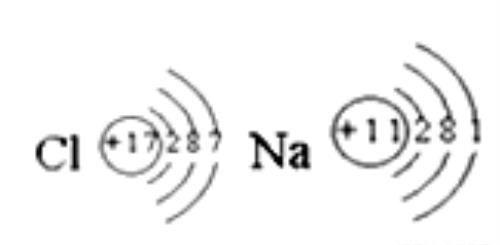

3 分类
带正电荷的离子叫做阳离子,一般由原子失电子形成;带负电荷的离子叫做阴离子,一般由原子得电子形成。
4 符号书写
离子
符号的主体是元素符号,在元素符号的右上角标上数字和正负号,用来表明离子所带电荷的数量和正负。书写的基本规则是数字在前,符号在后。

二、离子与其它粒子的区别与联系
1 离子与原子的区别与联系
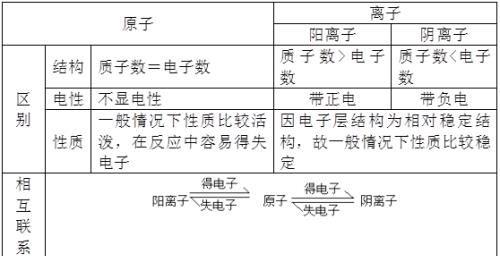
2 注意粒子与离子的区别
(1)粒子并不等同于离子,粒子的范围更广泛,包括分子、原子、离子等,则离子只是粒子的一部分。
(2)原子变成离子时,由于最外层电子数发生了变化,所以化学性质也发生了改变。
(3)具有稳定结构的粒子并不一定是离子,所以具有相同的电子层结构的粒子也并不一定是同一种粒子。

(1)原子得失电子变成离子后,变化的是其核外电子数,核内质子数没有变化,所以元素种类保持不变。形成离子所带的电荷数等于该原子(或原子团)得失的电子数。
(2)原子转化为离子,电子层结构可能发生变化。
①金属元素的原子,失去电子形成阳离子后,少了一个电子层;
②非金属元素的原子,得到电子形成阴离子,电子层数不变。
注意:具有相同的电子层结构的两种粒子,不一定是同种元素。
(3)同种元素所形成的离子,因其所带电荷不同,性质也不同,

典例剖析
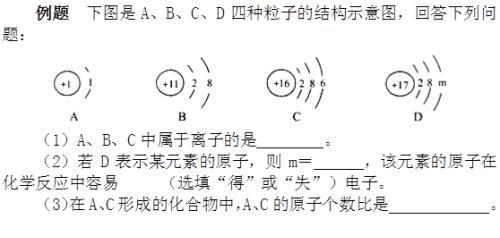
解析:离子是由原子得失电子形成的,其核外电子总数与核内质子数不等;阳离子的核
内质子数大于核外电子数,阴离子的核内质子数小于核外电子数,如果是原子,则核内质子数等于核外电子数,所以D原子的核外电子总数应该是17,因此m=17-10=7,若是A、C形成化合物,A的核外只有一个电子,可以失去一个电子,而C的最外层有6个电子,需要得到2个电子形成稳定结构,它们形成稳定化合物时,正负电荷的数目必须相等,故原子个数比应为2∶1。
答案:(1)B (2)7;得 (3)2∶1
点拨:电子是原子结构的一部分,不会凭空产生和消失,因此无论是分子中电子的转移还是离子中电子的得失,其总数必须相等,保证电荷守恒。
拓展提升
【方法提炼】
用等电子数法判断物质形成时的原子个数比
原子通过得失电子形成离子,离子是构成物质的基本粒子之一,阴离子和阳离子不能单独存在,它们彼此所带电荷不同,往往通过互相吸引形成稳定化合物。原子在形成离子时,电子不会凭空消失,也不会凭空产生,得失电子的过程其
实是电子的转移过程,所以在形成离子的过程中,得失的电子总数是相等的。解题时应用等电子数法往往可以使解题变得更为简单。
等电子数法的解题要领:
1 得失电子总数是相等的
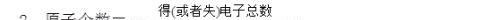


自我检测
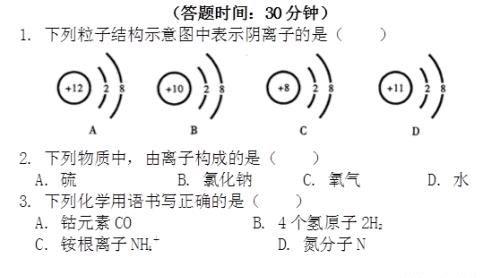

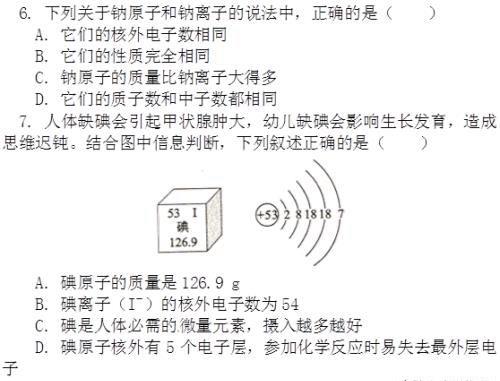
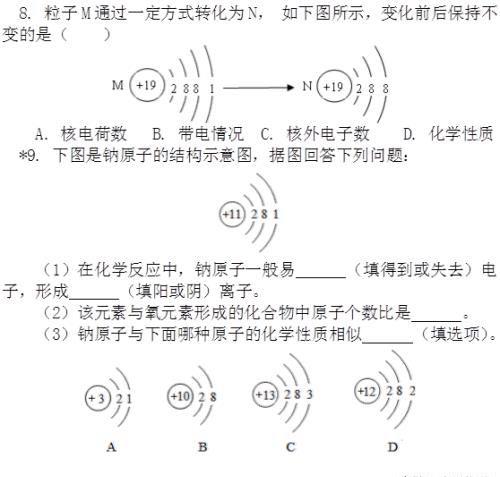
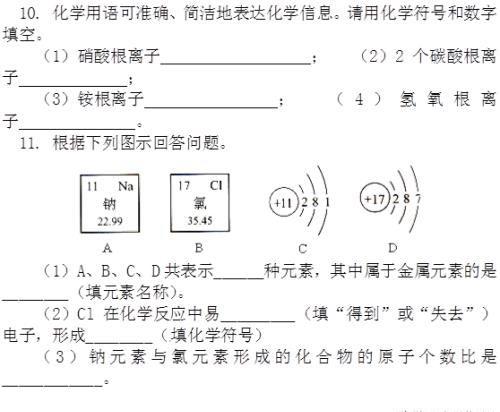
参考答案
1 C 解析:A中核内质子数大于核外电子数,属于阳离子;B中核内质子数等于核外电子数,属于原子;C中核内质子数小于核外电子数,属于阴离子;D中核内质子数大于核外电子数,属于阳离子,故选C。
2 B 解析:硫属于非金属固体单质,是由原子直接构成;氯化钠是由钠离子和氯离子构成;氧气是由氧分子构成;水是由水分子构成。

6 D 解析:金属原子易失去最外层电子形成具有相对稳定结构的阳离子,非金属原子得到电子形成具有相对稳定结构的阴离子,因此离子和原子的核外电子数不等,A错误;元素的化学性质与原子的最外层电子数关系密切。钠原子的最外层电子数没有达到相对稳定结构,在化学变化中表现为易失去电子,钠离子最外层达到相对稳定结构,B错误;原子的质量主要集中在原子核上,一个电子的质量非常小,因此钠原子和钠离子的质量差不多,C错误;原子形成离子的过程中质子数和中子数没有变化,D正确。
7 B 解析:根据碘在周期表中的信息可知,碘的原子序数为53,碘的相对原子质量为126.9,相对原子质量的单位不是质量单位,所以A不正确;碘原子最外层电子数为7,在化学反应中易得到电子形成碘离子,所以碘离子的核外电子数为54,即B正确;碘是人体必需的微量元素,但微量元素在体内有一个合理的浓度范围,高于或低于这一范围对人体健康都不利,所以C不正确;根据碘原子的结构示意图可知,碘原子核外有五个电子层,但在化学反应中易得到电子,所以D不正确。
8 A 解析:通过观察粒子M的结构示意图可以看出,M表示的是原子,最外层电子数为1,少于4个,在化学反应中易失去最外层电子变成离子,也就是
粒子N,在此过程中,原子核没有发生改变,所以核电荷数没有改变,故选项A正确;粒子M失去1个电子变成带1个单位正电荷的离子N,故选项B错误;粒子M变成粒子N,失去1个电子,故选项C错误;M的最外层电子数为1,而N的最外层电子数为8,故两者的化学性质不同,选项D错误。
9 失去;阳;2∶1;A
解析:钠原子最外层电子数为1,容易失去电子形成阳离子,离子形成稳定化合物时,得失电子总数是相等的,故钠原子和氯原子的个数比应为2∶1,原子的最外层电子数相同,化学性质相似,A中最外层电子数与钠原子相同。

12 (1)⑤;③ (2)③④⑤ (3)⑥
解析:原子得失电子形成离子,阳离子的核内质子数大于核外电子数,阴离子的核内质子数小于核外电子数;电子层结构
完全相同指的是电子层数相同,每一层容纳的电子数也完全一样,注意与粒子的种类无关,可以是原子,也可能是阴离子或阳离子;①的核外只有一个电子,只能转移或失去一个电子。要形成AB4型分子,则另一个原子的最外层电子数必须是4个,按照得失电子总数相等的原则,原子个数比为1∶4。
免责声明:本文内容由互联网优秀作者用户自发贡献,本站仅提供存储空间服务,不拥有所有权,不承担相关法律责任。若有涉嫌抄袭侵权/违法违规的内容,请与我们取得联系举报,一经查实立刻删除内容。本文内容由快快网络小面创作整理编辑!