无菌医疗器械包装试验方法(医疗器械无菌包装要求)
导语:怎么做无菌医疗器械的包装的运行确认OQ
为什么要做包装确认?
要保持无菌医疗器械的无菌,那么就需要有一个无菌屏障来保护已灭菌的器械,与外部环境隔绝,来保护器械。

无菌医疗器械
包装封口是无菌医疗器械生产过程中的一个非常重要的特殊过程,这个过程执行的好坏,直接影响到无菌医疗器械的性能、无菌保持和使用,从而影响到患者的安全。

连续式包装封口机
那么,这个包装封口过程的验证,是设计开发过程所要求的;同时,也是在提交产品的注册资料时,也是该产品的研究资料所要求的一部分,即产品的包装研究。
什么是包装封口的运行确认?
说通俗简单点,包装封口的运行确认,即是去寻找这个包装封口过程的关键参数范围,在这个关键参数范围内,生产出来的产品都是合格的。这些关键参数可能包括温度、时间、压力或者加热块的间隙值等。
如何去做包装封口的运行确认?
国内目前很多企业的运行确认看起来都比较简单,即选择或假设3组参数(中心值、上极限参数和下极限参数),分别对这3组参数进行封口一些样品,然后进行相应的测试,合格就算完成。
其实,要真正做好运行确认,即找好最优的参数,那么做好运行确认是非常有必要的;可以试试按以下流程进行:
1. 寻找参数
通过历史数据或者经验开始参数调试,直到找出低端参数和高端参数。每次调试都只能调整一个参数,其余参数固定。
低端参数的调试: 参数设置在历史经验参数范围的最低点。每个参数都往下进行调试,直到失效出现。当失效的参数出现后,再往回调,直至合格。高端参数的调试: 参数设置在历史经验参数范围的最高点。每个参数都往上进行调试,直到失效出现。当失效的参数出现后,再往回调,直至合格。当低端参数、高端参数确定后,那么这个过程的参数范围即可确定。
2 试验设计
对上一步骤所寻找的参数范围,我们可对其进行一个简单的试验设计。最简单的我们就用设计一个正交的试验对照。包含高、中、低三组参数。如下图:
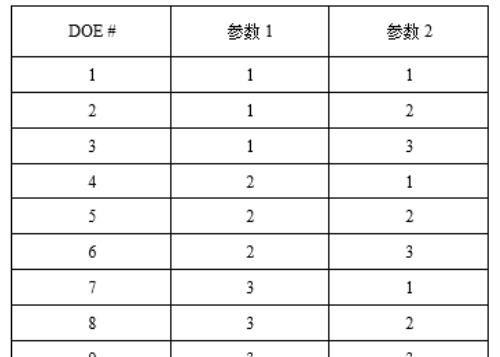
试验组次
此试验设计为9组次,对每一组进行运行,并取样进行测试。对所得的结果进行分析评估或打分,然后可利用Minitab软件对每个参数对结果的影响性来分析,比如生成一个主效应图,评估每个参数的影响性,从而得出最优的参数范围。
此步得出的最优参数范围,即是我们用来进行下一步性能确认的参数,也是我们写入生成作业指导书的参数。
3 参数挑战
在得出参数的极限范围后,为确保极限参数的更有效性。
那么对第一步骤的高、低极限参数进一步的挑战。
分别对高、低极限参数进行运行和取样,注意,取样的数量需要合理且具有充足的数量,才能进一步保障高、低参数的安全性。
完成运行确认
在参数范围、最优参数都找到后,那么我们可以根据运行的过程和结果从而形成运行确认的报告,经评审和批准后,运行确认即可完成。
欢迎做医疗器械相关工作的朋友一起留言讨论。
免责声明:本站部份内容由优秀作者和原创用户编辑投稿,本站仅提供存储服务,不拥有所有权,不承担法律责任。若涉嫌侵权/违法的,请反馈,一经查实立刻删除内容。本文内容由快快网络小悦创作整理编辑!